Опыты с электричеством еще не раз встретятся вам на этом сайте. Сейчас—самые простые. Чтобы провести их, достаточно трех-четырех батареек для карманного фонаря. Вообще-то опыты по электрохимии часто пытаются ставить дома, но не всегда они выходят: какая-нибудь мелочь — и ничего не получается. Если вы будете следовать всем нашим указаниям, можете быть уверены, что опыт удастся. Начнем с очень простого, но тем не менее поучительного опыта. Для него понадобится один-единственный реактив: чернила любого цвета. Правда, придется немного потрудиться над прибором. Возьмите две металлические полоски длиной 8—10 см и шириной 1—2 см. Они могут быть из железа, меди, алюминия — безразлично, лишь бы свободно проходили в прозрачный сосуд — высокую мензурку или большую пробирку. Перед опытом просверлите в пластинах с одной стороны отверстия для прикрепления проводников. Приготовьте две одинаковые, толщиной буквально в несколько миллиметров, пластмассовые или деревянные прокладки и склейте их с металлическими полосками так, чтобы те, расположившись параллельно, не касались друг друга. Клей годится практически любой — БФ, «Момент» и др. В мензурку или пробирку налей 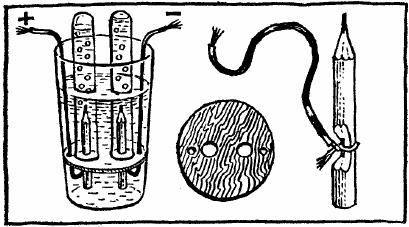 те воду и капните в нее столько чернил, чтобы раствор не был очень насыщенного цвета (однако он не должен быть и прозрачным). Опустите в него конструкцию из двух полосок, соедините их проводками с двумя батарейками, подключенными последовательно, «плюс» к «минусу». Несколько минут спустя, чернильный раствор между пластинками станет светлеть, а на дне и вверху будут собираться темные частицы. В состав чернила входят очень мелкие окрашенные частицы, взвешенные в воде. Под действием тока они слипаются и не могут уже плавать в воде, а опускаются на дно под действием силы тяжести. Понятно, что раствор при этом становится все более и более бледным. Но как же частицы попали наверх? При действии тока на растворы нередко образуются газы. В нашем случае газовые пузырьки подхватывают твердые частицы и уносят их наверх. В следующем опыте толстостенный чайный стакан, расширяющийся кверху, будет служить электролитической ванной. Приготовьте фанерный кружок такого диаметра, чтобы он прижался к стенке стакана в трех-четырех сантиметрах выше дна. В кружке заранее просверлите два отверстия (или вырежьте в нем по диаметру прорезь), неподалеку шилом проколите два отверстия: через них будут проходить проводки. В большие отверстия или в прорезь вставьте два карандаша длиной 5—6 см, очиненные с одного конца. Карандаши, точнее, их грифели, будут служить электродами. На неочиненных концах карандашей сделайте зарубки, чтобы обнажились грифели, и примотайте к ним оголенные концы проводков. Проводки скрутите и тщательно обмотайте изоляционной лентой, а чтобы изоляция была совсем надежной, лучше всего спрятать проводки в резиновых трубках. Все детали прибора готовы, остается только собрать его, т. е. вставить кружок с электродами внутрь стакана. Поставьте стакан на тарелку и налейте в него до краев раствор стиральной кальцинированной соды Na2CO3 из расчета 2—3 чайные ложки на стакан воды. Таким же раствором заполните две пробирки. Одну из них закройте большим пальцем, переверните вверх дном и погрузите в стакан так, чтобы в нее не попал ни один пузырек воздуха. Под водой наденьте пробирку на электрод-карандаш. Точно так же поступите со второй пробиркой. Батарейки — числом не менее трех — нужно соединить последовательно, «плюс» одной к «минусу» другой, а к крайним батарейкам подсоединить проводки от карандашей. Сразу начнется электролиз раствора. Положительно заряженные ионы водорода Н+ направятся к отрицательно заряженному электроду — катоду, присоединят там электрон и превратятся в газ водород. Когда у карандаша, подсоединенного к «минусу», соберется полная пробирка водорода, ее можно вынуть и, не переворачивая, поджечь газ. Он загорится с характерным звуком. У другого электрода, положительного (анода) выделяется кислород. Наполненную им пробирку закройте пальцем под водой, выньте из стакана, переверните и внесите тлеющую лучинку — она загорится. Итак, из воды Н2О получился и водород Н2, и кислород О2; а для чего же сода? Для ускорения опыта. Чистая вода очень плохо проводит электрический ток, электрохимическая реакция идет в ней слишком медленно. С тем же прибором можно поставить еще один опыт — электролиз насыщенного раствора поваренной соли NaCl. В этом случае одна пробирка наполнится бесцветным водородом, а другая — желто-зеленым газом. Это хлор, который образуется из поваренной соли. Хлор легко отдает свой заряд и первым выделяется на аноде. Пробирку с хлором, в которой находится также немного раствора соли, закройте пальцем под водой, переверните и встряхните, не отнимая пальца. В пробирке образуется раствор хлора — хлорная вода. У нее сильные отбеливающие свойства. Например, если добавить хлорную воду к бледно-синему раствору чернил, то он обесцветится. При электролизе поваренной соли образуется еще одно вещество — едкий натр. Эта щелочь остается в растворе, в чем можно убедиться, капнув в стакан возле отрицательного электрода немного раствора фенолфталеина или самодельного индикатора. Итак, мы получили в опыте сразу три ценных вещества — водород, хлор и едкий натр. Именно поэтому электролиз поваренной соли так широко используют в промышленности. С помощью тока и насыщенного раствора поваренной соли можно проделать еще один занимательный опыт. Займемся сейчас тем, что будем сверлить металл обыкновенным карандашом. Приготовьте в чайном блюдце насыщенный раствор поваренной соли. Соедините проводком лезвие безопасной бритвы с положительным полюсом батарейки для карманного фонаря (лезвие будет анодом). На заточенном конце карандаша обломайте грифель и примерно на полмиллиметра выковыряйте его иголкой. На 2—3 см выше сделайте ножом зарубку до грифеля и намотайте на нее конец оголенного провода; это место оберните изоляционной лентой, а другой конец провода присоедините к отрицательному полюсу батарейки (карандаш будет катодом). Положите лезвие в блюдце с раствором и коснитесь карандашом-катодом лезвия. Тотчас вокруг карандаша начнут бурно выделяться пузырьки водорода. А лезвие-анод будет растворяться: атомы железа приобретут заряд, превратятся в ионы и перейдут в раствор. Так минут через десять-пятнадцать в лезвии получится сквозное отверстие. Особенно быстро оно образуется, если батарейка новая, а лезвие тонкое (0,08 мм). В алюминиевой же фольге отверстие просверливается буквально за секунды. Если вы захотите просверлить карандашом отверстие в определенном месте тонкой металлической пластинки, то лучше заранее покрыть обрабатываемую деталь лаком, а там, где вы будете сверлить, лак снять. Углубление в грифеле понадобилось затем, чтобы грифель не касался металла. Иначе цепь сразу замкнется, ток не пойдет через раствор и никакого электролиза не будет. Сверлить карандашом можно и без электролитической ванны (в нашем случае, без чайного блюдца). Пластинку-анод положите на доску или на тарелку, капните воды, обмакните карандаш, присоединенный к батарейке, в соль и погрузите заточенный его конец в каплю. Время от времени удаляйте тряпочкой продукты электролиза и наносите новую каплю. Повторяя эту операцию, можно, не прикладывая усилий, просверлить металлическую фольгу или жесть от консервной банки. Так же, между прочим, можно сделать отверстие в сломанном стальном ноже, чтобы приделать к нему новую ручку.
Конечно, для сверления металла толщиной более миллиметра одной батарейки мало — надо включить параллельно несколько батареек или воспользоваться понижающим трансформатором с выпрямителем — например, от детской железной дороги или от прибора для выжигания по дереву. И независимо от источника тока и способа электролиза придется несколько раз менять раствор электролита и хорошо очищать лунку— гвоздем или шилом.
О.Ольгин "Опыты без взрывов"
|